
文献综述
国产崛起,填补空白 1月两款ECMO获批, 危重患者的“终极武器” 从研发到临床 ——多维度还原救命神器 期待国产技术迎来更多高光时刻引言
“2023年1月,国家药监局应急批准汉诺医疗(1.4日)和长征医疗(1.17日)的ECMO产品(体外肺/心肺支持辅助设备)上市,系国内首款和第二款获批的国产ECMO设备,填补了国内空白。”
体外膜肺氧合
Extracorporeal Membrane Oxygenation,ECMO
又称“人工肺、叶克膜”,一种重要的体外生命支持技术,将患者的部分静脉血从体内引到体外,经膜肺氧合后再由驱动泵将血液回输体内,对严重循环、呼吸衰竭的病人进行有效支持,主要用于心脏功能不全、呼吸功能不全的支持,被誉为ICU里把守“生死之门”的最后一道防线,抢救新冠肺炎危重病人的“终极武器”,ECMO作为常规治疗无效的危重型新冠肺炎患者的挽救性治疗设备,是《新型冠状病毒肺炎诊疗方案》中明确的治疗措施,但受制于研发难、生产难、技术门槛高、临床使用制约等多因素限制,国产企业无ECMO设备获批上市,我国ECMO严重依赖进口,主要被美敦力(Medtronic)、理诺珐(LivaNova)和迈维柯(Maquet)三家垄断。
ECMO的临床落地
 离心泵和膜肺是ECMO的两大核心构件,分别起到人工心脏和人工肺的作用,是最具技术研发难度的部分,也是当前ECMO国产化的难点。而临床试验的难点在于试验方案设计面临无从参考的困难,国内尚无ECMO审批的技术指导原则,且此前没有获批的产品,故没有临床试验的经验可供借鉴。目前公开数据查询到的临床试验方案设计有“前瞻性、多中心、随机、单盲、阳性平行对照”及“前瞻性、多中心、单组目标值”两种,试验一般在医院的重症监护室(ICU♛)入组受试者,根据在阜外医院开展的一项临床试验方案显示,方案要𓂃求入组28例患者,存活率达50%以上。
离心泵和膜肺是ECMO的两大核心构件,分别起到人工心脏和人工肺的作用,是最具技术研发难度的部分,也是当前ECMO国产化的难点。而临床试验的难点在于试验方案设计面临无从参考的困难,国内尚无ECMO审批的技术指导原则,且此前没有获批的产品,故没有临床试验的经验可供借鉴。目前公开数据查询到的临床试验方案设计有“前瞻性、多中心、随机、单盲、阳性平行对照”及“前瞻性、多中心、单组目标值”两种,试验一般在医院的重症监护室(ICU♛)入组受试者,根据在阜外医院开展的一项临床试验方案显示,方案要𓂃求入组28例患者,存活率达50%以上。
国内ECMO产品研发进度

主要研发企业
 何为应急审批?
何为应急审批?
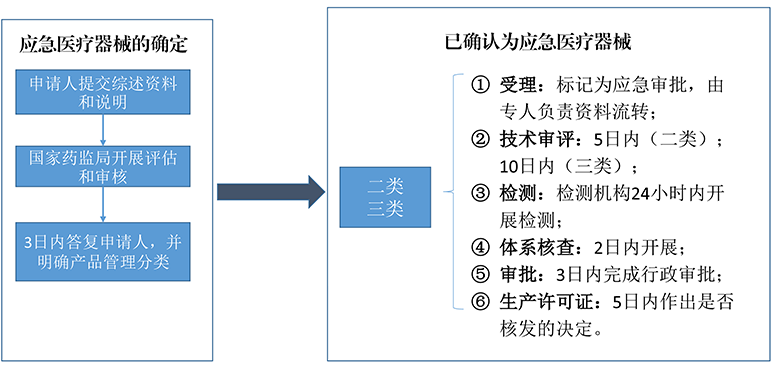
两款ECMO均为应急批准,应急审批是指当社会存在突发公共卫生事件威胁以及突发公共卫生事件发生时,为有效预防、及时控制和消除突发公共卫生事件危害,确保应急所需医疗器械能够尽快完成注册审批的程序。在产品注册申报过程中,国家药监局按照“统一指挥、早期介入、快速高效、科学审批”的原则,成立应急审评工作组,专人负责、全程指导、发布技术审查指导原则,加大产品注册申报指导,加快审评审批进程,在保证安全、有效的基础上推动产品尽快上市。截至2022年12月22日CMDE统计,自2020年1月以来,已有170个产品经应急审批上市。

专家共识&指导原则
热点赛道,蓄势待发
- END -
【关于世界杯压球 】
世界杯压球 解散于2004年,谋生物药业行业中领域可以提供了CRO&CDMO合二为一化世界杯压球 。机构倾力为药业行业中领域MA化解设计方案设计领导人员者,为安全管理事业上的不断创建新的餐饮市场价值。群体用可以提供了期限性强、生产成本人工控制、货品的有有保险和职业性的研究分析建设、货品的探测、哺乳动物实验报告、临床治疗试验检测和货品的注册成功分钟化解设计方案设计,不断推进安全管理、有郊和货品的人工控制的货品的进来餐饮市场,有保险社会生命图片安全管理。 具体位置:首都市丰台区南四环西路1810号汉威國際城市广场二区2号楼7层 座机号:400-080-9519;010-83739181 qq邮件:services@hibalag.com 站点://hibalag.com